Introduktion
Förbudet eller förkastandet av användningen av antibiotiska tillväxtfrämjare (AGP) i fjäderfäfoder i många länder samt de ökande restriktionerna för användningen av antibiotika terapeutiskt leder till ett nytt paradigm där termer som "tarmhälsa" eller "alternativ till antibiotika" har blivit mycket vanliga i det samlade lexikonet för fjäderfäindustrin och forskningen. Frånvaron av AGP i fodret exponerar verkligen underliggande tarmproblem som inte nödvändigtvis är relaterade till infektioner utan till inflammatoriska svar på kostfaktorer.
I vår tid, det finns många fodertillsatser utvecklade med motivationen att ersätta AGP. Dock, även med de många tänkbara tillsatsblandningar, sammansättningen av den basala kosten och kvaliteten på dess ingredienser spelar utan tvekan en huvudroll i AGP-fria produktionssystem. I detta sammanhang, kvaliteten på sojamjöl (SBM), en nyckelingrediens i alla fjäderfäfoder globalt, och dess bidrag av antinäringsfaktorer (ANF) i foder kan i hög grad efterfråga tarmens funktion och hälsa och, följaktligen, kycklingars utveckling och tillväxt.
I den här artikeln, vi kommer att se över hur kostkomponenter kan vara orsaken till tarmproblem hos kycklingar och verkningsmekanismen för AGP genom vilken de täcker upp dessa problem. I nästa nummer av The Poultry Site, vi kommer att ta upp vikten av att minska sojaantinäringsfaktorer i kycklingfoder, när vi inte längre har AGP.
Inflammation och oxidativ stress är roten till tarmsjukdomar hos kycklingar
Inflammatoriska reaktioner och oxidativ stress är involverade i vanliga tarmsjukdomar hos slaktkycklingar. Tarminflammation är faktiskt ett generiskt svar på den medfödda immuniteten, en del av det komplexa värdförsvarssystemet mot skadliga stimuli. Det är viktigt att notera att tarminflammationer hos kycklingar inte bara beror på infektioner. Således, Kogut et al (2018) påpekade att, förutom akuta patologiska inflammationer (på grund av infektioner), en av de mest återkommande typerna av tarminflammation hos kycklingar är steril inflammation. Detta är en låggradig kronisk inflammation på grund av icke-infektiösa stimuli, och för det mesta till vissa ANF som finns i fodret. I det här sammanhanget, det har visat sig att antigenet beta-konglycinin, finns i sojamjöl, såväl som spannmålsgluten prolaminer kan leda till tarminflammation. Detta verkar förmedlas av ett ökat uttryck och produktion av flera pro-inflammatoriska cytokiner i tarmen, förändrat uttryck av tight junction-proteiner i tarmepitel, och apoptos (Chen et al, 2011; De Punder och Pruiboom, 2015; Peng et al, 2018). Andra utlösande faktorer för steril inflammation av kosten är lipider med en viss härskning, som är en viktig källa till reaktiva syrearter (ROS) som är kraftfulla inducerare av inflammation i slemhinnan, som det nämns senare i denna artikel. Således, kvaliteten på fetter och oljor som tillsätts foder, samt kvaliteten på alla dessa råmaterial av animaliskt ursprung med hög lipidhalt (t.ex. fisk måltid, fjäderfäbiproduktmjöl) kan spela en relevant roll i uppkomsten av foderinducerade sterila inflammationer (Mavromichalis, 2019).
Under det inflammatoriska svaret, fagocytiska immunceller producerar fria radikaler som ROS och reaktiva kvävearter (RNS, t.ex. kväveoxid), vid aktivering av de oxidativa enzymerna NADPH-oxidas (NOX) och kväveoxidsyntas (iNOS), respektive, båda inducerade av pro-inflammatoriska cytokiner som utsöndras inom ramen för den inflammatoriska processen (Tian et al., 2017). Således, alla typer av tarminflammation kommer att generera ROS och NOS, vilket kommer att leda till ett tillstånd av oxidativ stress i tarmen. Dessa fria radikaler uppvisar antimikrobiella egenskaper men kan också orsaka vävnadsskador under inflammation. I detta avseende ROS och RNS är båda huvudmediatorer ansvariga för de intracellulära skadorna av kolhydrater, proteiner, lipider, och nukleinsyror, är mycket reaktiva på grund av deras instabila förhållanden med oparade elektroner (Lauridsen, 2019).
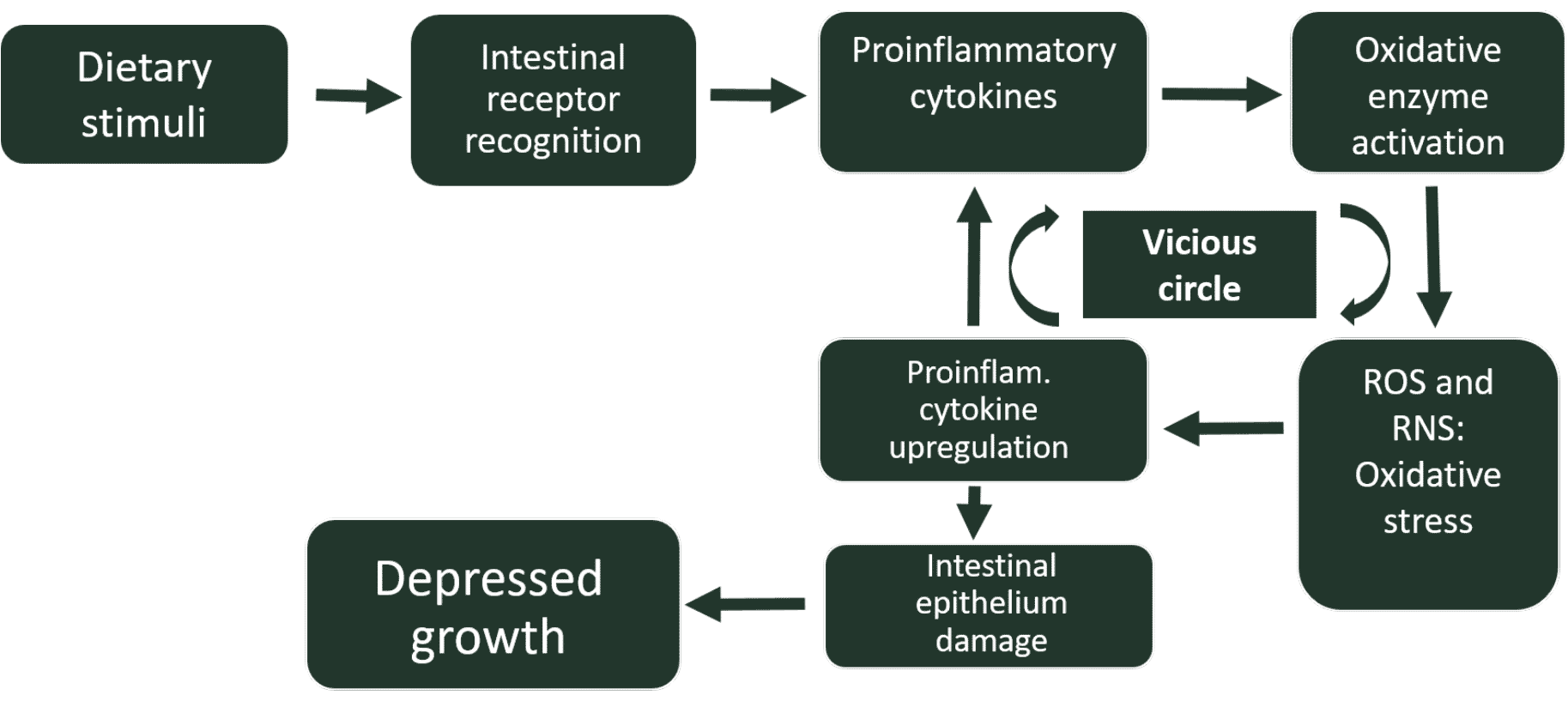
Vidare, denna inflammationsassocierade oxidativa stress kan modifiera fenotypen hos flera celler, vilket resulterar i förändringar i uttrycket av vissa gener. Till exempel, under förhållanden av oxidativ stress i tarmen, det finns en uppreglering av uttrycket av flera pro-inflammatoriska cytokiner, samt en nedreglering av occludin och mucin 2, molekyler som ansvarar för integriteten hos tarmepitel (Ducatelle et al. 2018). Således, oxidativ stress som genereras under tarminflammationer kommer att öka svårighetsgraden av dessa inflammationer, går in i en ond cirkel, svårt att övervinna, vilket kommer att leda till upprättandet av ett kroniskt inflammatoriskt tillstånd, med betydande oönskade biologiska konsekvenser såsom tillväxtförfall (Figur 1). Å andra sidan, som tidigare nämnt, inflammation som härrör från och inducerar oxidativ stress kan förvärras ännu mer genom att inkludera foderingredienser av animaliskt ursprung som är rika på härskna fetter, vilket kommer att initiera en ytterligare oxidationskaskad i kycklingens tarm, öka utsöndringen av proinflammatoriska cytokiner.
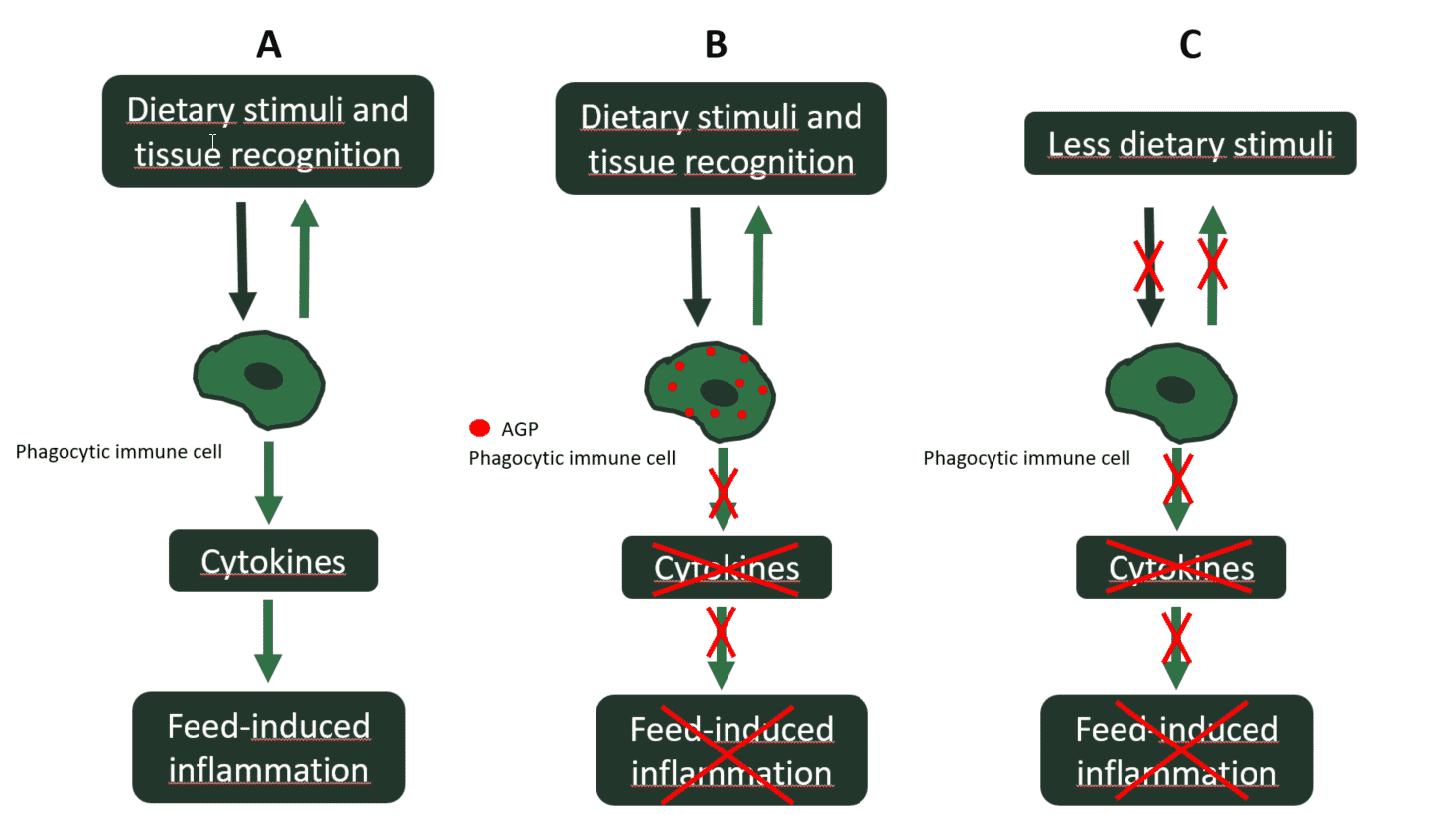
Denna typ av tarmsjukdomar är mer framträdande hos kycklingar som tidigare var naiva mot inflammationsframkallande foderingredienser. Därför, unga kycklingar reagerar genom ett inflammationssvar som kan komma att bli komplicerat av opportunistiska bakteriepatogener som finns i deras omogna tarm. Dock, när AGP läggs till i flödet, sådana foderinducerade inflammatoriska svar mildras av den antiinflammatoriska effekten av AGP.
Antiinflammatorisk effekt av AGP
På senare år har den antimikrobiella effekten av AGP har ifrågasatts, eftersom koncentrationerna de når i tarmens lumen är subterapeutiska och därför lägre än de lägsta hämmande koncentrationerna för patogener. Vidare, oavbruten användning av AGP inducerar antibiotikaresistens hos patogener. Tvärtom, den antiinflammatoriska effekten av AGP, som deras huvudsakliga verkningsmekanism, har fått aktualitet. Vad många antibiotika verkligen har gemensamt är att de ackumuleras i inflammatoriska celler. Följaktligen, de flesta ackumulerade antibiotika kan hämma fagocytiska inflammatoriska celler av det medfödda immunsvaret i tarmen. Det relevanta resultatet av denna ackumulering i fagocytiska celler är minskningen av det inflammatoriska svaret. Därför, nivåerna av pro-inflammatoriska cytokiner är lägre hos AGP-behandlade djur, vilket i sin tur kommer att resultera i lägre katabolisk inducering, typiskt för inflammation (Niewold, 2007). Med andra ord, AGP hämmar inflammatoriska svar som bromsar tillväxten av kycklingar. Därför, när det inte finns någon AGP i flödet, de foderinducerade sterila inflammationerna återkommer. En bra strategi är att försöka minimera förekomsten av sådana foderinducerade inflammationer i förväg genom att minska mängden dietstimuli (t.ex. ANF) i basalien, istället för att mildra dem med AGP när de väl har slagit sig ner i tarmen (Figur 2).
Sammanfattningsvis, foderinducerade sterila inflammationer och oxidativ stress hos kycklingar kan komma från en hel del ingredienser. Den resulterande inflammationsoxidativa stressens onda cirkel försämrar hälsa och prestation. Därför, vi bör se till att vårt AGP-fria foder inte innehåller ingredienser som sannolikt stimulerar inflammation eller, åtminstone, vi måste minska mängden antinäringsfaktorer i fodret så mycket som möjligt. Detta är särskilt viktigt i (för-)startfoder. Ju tidigare vi kväver den ovan nämnda onda cirkeln i sin linda, desto bättre.